どーも、ききです。
遂に学識まで来ました。こちらでは多数の計算問題が出てきますが
正直かなり難しいです
ですが、自分なりに考えた簡単に解ける方法をなど伝授します。
普通に解くと物凄く時間が掛かるので…学識は特に時間を掛けてじっくり勉強しました。
ではさっそく初めていきます。
単位

ここから一気に数字との闘いになります。あとは暗記。
化学とか数学が得意な人なら案外取っつきやすいかもしれません。
- t=T-273.15(tはセルシウス度、Tは熱力学温度)
- 1Mpa=1,000kpa=10,000hpa=1,000,000pa
- P=Pa+Pg(P=絶対圧力、Pa=大気圧、Pg=ゲージ圧力)
- 1秒当たりに移動するエネルギーが1Jである時の仕事率は1W
- 1Nの力で物体を1m動かす仕事が1J
- 1㎡の面に1Nの力が垂直で均一に掛かる時の圧力が1Pa
特に赤字は必ず覚えて下さい。
この後の計算問題で嫌ってくらい出てきます。

ちなみに問題は
①T=t-273.15は正しいか、②Pa=P-Pgは正しいか
みたいな感じで出題します。上の問題だと①はTとtが逆なので不正解、②は分かりにくいですがPgを左辺に移動するとPa+Pg=Pとなるので正解です。
セルシウス温度27℃は熱力学温度で表すと310.15℃である
この問題は上のリストを参考に数字を当てはめると
T=273.15+27=300.1となるので不正解です。
まだ始まったばかりですが、ここまで大丈夫ですか?
僕はもうお手上げです(コラ

原子 分子 元素 理想気体 計算問題
ここではまず化合物か単体かを覚える必要があります。
簡単なものでいうと
- メタン(CH4)、プロパン(C3H8)等は化合物
- ヘリウム(He)、酸素(O2)、窒素(N2)等は単体
ようは元素記号で二つ以上のものは化合物、一つのものは単体と覚えます。
今は良く分からなくてもこの後、嫌ってくらい出てくるので自然に覚えると思います。
また、文面として
- 1molの物質は6.02x1023個の基本粒子が含まれる。これをアボガドロ定数
- アボガドロ定数によれば、全ての気体において、同じ温度、同じ圧力のもので、同じ体積中に含まれる分子の数は常に同じ
- アボガドロの法則は全ての気体1molは標準状態でおよそ22.4ℓの体積を占める
理想気体については
- 温度が一定なら気体の体積は絶対圧力に反比例
- 圧力が一定なら一定量の気体の体積は熱力学温度に比例
- (PV/T)
遂にここで計算問題を解いていきます。
まずはこの問題
6kgの液体プロパンが気化して気体になった。この気体のプロパンの体積は標準状態(0℃、標準大気圧)でおよそ何㎥か。ただしプロパンの分子量は44とし、理想気体として計算せよ。
頭痛くなりそうな問題ですね。
まだまだこんな感じの問題は続きますが(悪夢
解き方として一つ式を覚えます
質量÷分子量x22.4=体積
あとは問題文の赤文字をこの式に入れていくだけです。
6÷44x22.4=約3.1㎥
となります。少し違う問題だと
標準状態(0℃、標準)で10㎥を占める窒素ガスの質量はおよそ何kgか。ただし窒素の原子量は14とする
この問題は少し式が違うだけで基本的には解き方は同じです。
また、この問題は原子量で記載されているので分子量に置き換えて計算します。
今度は質量を求めるので
分子量÷22.4x体積=質量
となるので上の赤字の所を挿入して
(14x2)÷22.4x10=12.5kg
となります。
次の問題は
密閉容器内の温度を20℃から60℃に上昇させると、容器内の気体の絶対圧力は20℃の時の絶対圧力の3倍になる。
この問題は上のリストのPV/Tに当てはめると解けますが、この手の問題は大体1.1倍前後になります。なのでこの問題文は不正解です。
良く分からなくても、今はとりあえずそう覚えましょう。

念のため計算式を書いておきます。この解き方は次の問題でも活躍します。
- P1xV1/T1=P2xV2/T1
- V1=V2なので
- P1/T1=P2/T2
- P2(上昇後の圧力)=P1xT2/T1
- P2=P1x(60+273.15)/(20+273.15)
- P2=P1x1.1
次の問題が
メタンを真空容器に25℃で0.2Mpa(ゲージ圧力)まで充填した。温度が75℃になると、容器内の圧力(ゲージ圧力)はおよそいくらになるか。ただしメタンは理想気体とし大気圧は標準大気圧として計算せよ
まず式はP1V1/T1=P2V2/T2として、同じ容器なのでV1=V2を前提に解いていきます。
また、問題文がゲージ圧力なのも注意します。
P=ゲージ圧力+大気圧、T=セルシウス度+273.15℃なので
- P1/T1=P2/T2
- P2=P1xT2/T1
- P2=(01+02)x(75+273.15)÷(25+273.15)
- P2=0.35
- ゲージ圧力では
- 0.35-0.1(大気圧)=0.25Mpa
となります。次の問題は
温度30℃で内容積20ℓの真空の容器に酸素ガスを充填したところ、圧力が2Mpa(ゲージ圧力)となった。およそ何molの酸素ガスが充填されたか理想気体として計算せよ
充填されたか求める問題では次の式を覚えます。
PV=nRT(R=8.3145)n=充填量
そして上の問題文の赤字の数字を挿入して
- (2+0.1)x20=nx8.3145x(30+273.15)
- n=約16.7mol
となります。
ここまで少し難しいと思ったかもしれませんが似たような問題を反復して解いていくと案外身に付きます。
あと、この辺の問題はこの後に出る計算式より少し簡単な部類だと思うので、ここでつまづいてはいけません。
とりあえず赤字のところだけは必ず覚えましょう。

純物質の性質、状態変化、臨界状態 純物質の飽和蒸気圧
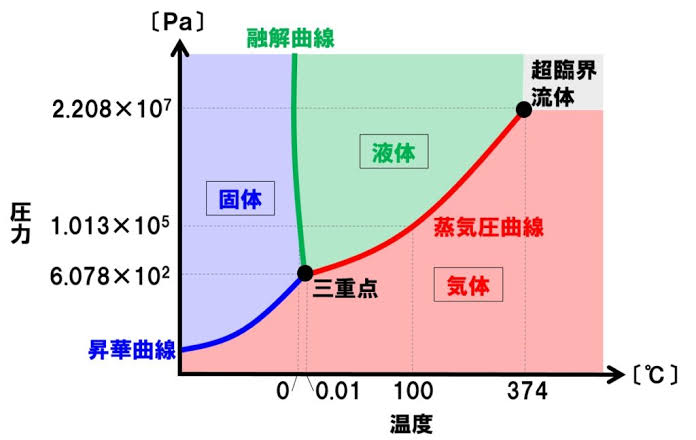
状態図についてはこちらをご覧ください。
引用:大学受験対策ポイント解説サイト
- 圧力、温度による固相、液相、気相間の状態変化を表したものを状態図という
- 固体から液体は融解、液体から気体は気化
- 気体から液体は凝縮、液体から個体は凝固
- 固体から気体は昇華、気体から固体も昇華
- 固相、液相、気相が平衡を保って同時に存在する点を三重点
- AOは昇華曲線、OCは蒸発曲線、OBは融解曲線
- 相変化のみに使われる熱量を潜熱
- 物質の温度の上下に関係する熱量を顕熱
飽和蒸気圧については
- 飽和蒸気圧は温度の上昇と共に上昇する
- 液量は関係ない
- 沸点は液体の飽和蒸気圧が液面上の全圧に等しくなる温度
沸点についてですが、こちらはガチの暗記になります。
でも細かい数字を完璧に覚える必要はないので安心して下さい。
とにかく赤字の数字で覚えて下さい。
カッコ内が正確な数値です。良く出るものだけ厳選します。
- 窒素 -200℃(-195.8℃)
- 水素 -250℃(-252.9℃)
- ヘリウム -270℃(-268.9℃)
- メタン -160℃(-161.5℃)
- エチレン -100℃(-103.7℃)
- プロパン -40℃(-42.1℃)
- 酸素 -180℃(-183℃)
- アンモニア -30℃(-33.4℃)
- ブタン -0.5℃
ちょっと長いですが、この後でまた違う数値を覚えなければいけません(は
少しでも覚えやすいようにしたつもりなので頑張って暗記しましょう。
化学反応(燃焼計算、燃焼反応式)

まずはこの問題
次の式はプロパンが完全燃焼する時の化学反応式である。()内に入れる数値はどれか C3H8+(A)O2→(B)CO2+(C)H2O
この問題は左側の式と右側の式の係数を見て解きます。
左側のCは3なので右側の(B)は3です。左側のHは8なので右側の(C)は4です。あとは右側のOの係数を整理して左側の(A)は5です。
では次の問題
次の式はアンモニア合成反応の熱化学方程式です。次の反応のうちこの反応について正しいものはどれか 1/2N2+3/2H2=NH3+45.9kJ
①一定の圧力下で温度を高くすると、アンモニアの平衡濃度は高くなる
②一定の温度下で圧力を高くすると、アンモニアの平衡濃度は低くなる
③アンモニアの合成反応は、発熱反応である
この問題は理想気体のところで出てきた圧力と温度の関係を逆にして覚えます。つまり
- 圧力が一定→濃度は反比例
- 温度が一定→濃度は比例
なので①は不正解、②も不正解です。
また、③は右側の式が+が発熱反応、-が吸熱反応となります。
なので③は正解です。
次の問題は
次の式はメタンが完全燃焼する時の反応式である CH4+2O2→CO2+2H2O 1㎥の気体のメタンを上式に従って理論上完全燃焼させる為の最小必要空気量(完全燃焼組成の空気量)はおよそ何㎥か。ただし空気中の酸素濃度は21vol%とする
何書いてあるか良く分かりませんが、この問題は酸素の係数2を酸素濃度で割ると求められます。
- 2÷0.21=9.5㎥
となります。余計な事は考えずにこの解き方だけ覚えましょう。
最後に熱量計算です。問題は
温度20℃の水10kgを標準大気圧下で沸騰させ、全て気化させるにはおよそ何kJの熱が必要であるか。ただし、水の比熱容量は4.19kJ、水の蒸発熱は2,260kJとする
この問題も余計な事を考えずに解き方だけ覚えます。
まず、水の沸点は100℃なのでその温度差と比熱容量、質量を掛けます。
それと別に質量と蒸発熱を掛けてそれぞれを足します。
- (100-20)x10x4.19+10x2,260=約26,000kJ
となります。
この手の問題は全て解き方さえ分かれば必ず答えに辿りつけるので頑張って解いてみてください。
計算ばかりで少し疲れてきましたね…でも安心して下さい。
次は暗記系です(まじかよ
燃焼、爆発
一般に温度の上昇とともに爆発下限界は低下する(爆発上限界は上昇)つまり、爆発範囲が広くなります。
可燃性ガスに不活性ガスを添加して、酸素濃度を限界酸素濃度より低く保っている状態では可燃性ガスの濃度が高くなっても混合ガスは爆発範囲に入らない。
ここから最小発火エネルギーの最低値と爆発下限界の数値を覚えていきます。
正直、沸点もそうですがどれが出るか分からないので全て暗記する必要があります。赤字が最小発火エネルギー、青字が爆発下限界です
- 水素 1.6 4
- アンモニア 1,400 15
- メタン 28 5
- ブタン 25 1.8
- プロパン 25 2.1
- エタン 25 3
- アセチレン 1.8 2.5
とりあえずここまで覚えましょう(白目)

ガスの性質 工業的製造法
ここではガスの性質についての問題が出てきますが、全てのガスの性質を覚えるのはかなりしんどいので良く出題されるところだけ厳選します
- 塩素と酸素(水素)の体積比が2:1は塩素が爆鳴気と呼ばれ爆発的に反応する
- 二酸化炭素は不燃性で大気圧では低温にしても液化せずに直接固体になる
- アセチレンは溶接に使用される
- 空気の分子量は29(この値を覚えておくと空気より軽いか重いか分かる)
- 水素と塩素は還元性物質
工業的製造法については
- アセチレンはカルシウムカーバイト
- 窒素、酸素、アルゴンは液化分離法、吸着分離法
- 水素は水蒸気改質法
- 塩素は食塩水の電気分解
- エチレンはナフサ(炭化水素)の熱分解
- アンモニアは化学平衡的に有利な高い圧力下で、窒素と水素の発熱反応で製造
- 一酸化炭素は副生ガスから回収
ここまで覚えておけば大丈夫です(多分)
円管内の流体の流動 伝熱
ここで覚えておく事は
- レイノズル数が2,100以下は層流、4,000以上は乱流
- レイノズル数は粘度に反比例する
- ファニングの式は内径に反比例する。流体の摩擦によるエネルギー損失を求める。
- 流れの状態が乱流である場合、平均流速が2倍になると、管摩擦係数を一定とすれば摩擦によるエネルギー損失は4倍になる
- 一般に液体輸送は乱流域で行われるが、粘度が高い液体では層流域で輸送される事が多い
伝熱では
- 固体壁を隔てて高温の液体から低温の液体に熱が移動する伝熱を熱伝達
- 固体内の伝熱を伝導伝熱
- 流体の流れにより熱エネルギーが運ばれて起こる移動を、対流伝熱
- 放射伝熱は熱を伝えるのに媒体を必要とせず、高温の炉などではこの伝熱が支配的となる
- 多孔質物質の保温材が濡れて細孔内に水が浸入すると、保温能力は低下する
- 熱放射線を反射も浸過もなく全て吸収する仮想的、理想的な物体は黒体
- 黒体から放射される熱放射エネルギーの大きさはケルビン度(K)で表したその黒体の温度の4乗に比例する
熱伝導率は
銅>アルミニウム>炭素鋼>18-8ステンレス>水>ポリエチレン>空気
ここまで覚える。
応力とひずみ 応力の計算
応力とひずみでは
- 縦軸は応力(σ)、横軸はひずみ(ε)
- A点は比例限度、B点は弾性限度、C点は上降伏点、DE点は下降伏点、F点は極限(引張)強さ、G点は破壊応力
- 荷重の小さい範囲えは応力とひずみは比例しσ=Eεと表す。比例定数をEをヤング率という
- 引張試験を行い破断した試験片の変形具合から絞りを求める事が出来、破断後の最小断面積と元の断面積から算出した断面積の減少率を%で表したもの
次は恐怖の計算問題です(苦)
でも、ここでの計算問題が学識での最後の計算問題になります。なので気合いれていきましょう。
まずは問題
長さ5m、直径120mmの一陽な断面を持つ軟鋼製丸棒に300kNの引張荷重を掛けた時、およそ何mmの伸びが生じるか。ただし、丸棒の縦弾性係数を210GPaとする
この問題ではまず棒の断面積を求めますが120mmを0.12mとして
・3.14x(0.12)2÷4=約0.0113㎡
ここでひずみを計算して、伸びを求めていきますが過去問解き方(おそらく正式な解き方)は
良く分からない式になり、自分も正直良く意味が分かりません(汗)
しかも210GPaは計算すると210⁹というかなり大きな数字になり計算が非常にめんどくさいです。
なので、我流で考えた式を使います。
引張荷重÷断面積÷縦弾性係数x長さ÷1,000
この計算式に当てはめると
300÷0.0113÷210x5÷1,000=約0.63mm
と割と簡単に解けます。一応下に過去問の解説の解き方を書いておくので参考までに…
ε=σ/E=(300x103N/0.0113㎡)/(210x10^9Pa)=1.26x10-4
λ=εL=1.26x10-4x5.0m=0.63mm
もう一つの問題は
直径26mmの一様な断面を持つ鋼製丸棒に95kNの引張荷重を掛けた時、丸棒の断面にはおよそ何MPaの応力が生じるか
(1)45MPa(2)65MPa(3)90MPa (4)135MPa (5)180MPa
この問題も先に断面積を求めて純粋に荷重から割れば求められます。
・0.026x0.026x3.14÷4=約0.00053㎡
・95÷0.00053=179,245KPa
KPaをMPaに変換すると
179,245÷1,000=約180MPa
となります。
以上で計算問題は終わりです。お疲れ様でした。
しかし、もう少し覚える事があるのでもうひと踏ん張り頑張りましょう(嫌)
zzz…
金属材料の強度と破壊 炭素鋼、ステンレス鋼 金属の腐食
- 延性破壊は大きな塑性変形が生じ、脆性破壊は塑性変形を生じない
- 疲労に関する性質は縦軸に応力の振幅S、横軸に破壊するまでの繰り返し数NによるS-N曲線
- クリープ曲線は縦軸にひずみ、横軸に時間
- 棒に切欠きがある場合、応力は切欠き部に近づくと急激に増大して切欠き底部で最大となる。このように形状が変化する部分で応力の大きい部分が生じる現象を応力集中
- 材料の許容応力は、基準強さ÷安全率
炭素鋼については
- リンや硫黄の含有量が多いと溶接性が悪くなる
- 炭素の含有量は0.02~2%
- 含有量が増えると引っ張り強さ、降伏点、硬さが大きくなり伸び、絞りが小さくなる。溶接性も低下する。
- 焼き戻しは靭性改善、焼きならしは組織を微細化する、焼きなましは内部歪みを除去し軟化させる
ステンレスは
- 18-8ステンレス鋼はクロム18%、ニッケル8%
- 18-8ステンレス鋼は磁性を持たないが13クロムステンレス鋼は磁性有り
- 18-8ステンレス鋼は高温強度に優れ、低温脆性が起きない
金属の腐食については
- 応力腐食割れは引張応力下にある金属が腐食環境中で割れを生じる
- 環境のpHは腐食に影響を及ぼす
- 腐食環境下で材料が腐食する事をエロージョン、乱流やスラリーの衝突による損傷をコロージョン
- 引張応力下にあるSUS404は60℃以上の多量の塩化物イオンを含む環境で応力腐食割れを起こす
防食と腐食に関しては保安管理技術で記事を書いているので割愛します。
溶接、溶接欠陥 計測器
ここでは問題文のキーワードを見つけて問題を解いていきます。細かい事は覚えなくて良いです。まずは溶接の種類から
- ティグ溶接はタングステン、不活性ガス
- サブマージアーク溶接はあらかじめ~
- 被覆アーク溶接は被覆アーク溶接棒
- ミグ溶接は大気から保護
溶接欠陥については
- アンダカットは母材が掘られる
- オーバーラップは母体に融合しないで重なる
- 溶け込み不良は溶け込まない部分がある
- 融合不良は十分に溶け合ってない
- スラグ巻込みはスラグが残る
他には気孔やビード下割れなどありますがここまで覚えれば大丈夫でしょう
計測器については
- バイメタル式温度計は熱膨張率の小さい方に曲がる
- ブルドン管圧力計は他端を密閉して自由に動ける構造
- ディスプレーサ式液面計はディスプレーサの浮力を利用
- オリフィス流量計はオリフィス板の直近の上流と下流とで圧力に差が生じる
- 抵抗温度計は電気抵抗が温度によって変化する事を利用している
- 磁気式酸素系は酸素の濃度を測定
ガス圧縮 ポンプ
ガス圧縮では
- 等温圧縮において取り去る必要のある熱量は、圧縮の為に外部から加えられた仕事に相当する熱量となる
- 圧縮に要する仕事は等温圧縮<断熱圧縮
- 実際の圧縮はポリトロープ圧縮となりpV^n=一定となり、1<n<γとなる
- 断熱圧縮ではガス温度は上昇する
- ガスを圧縮する場合は圧縮に要する仕事を小さくする為に出来るだけ等温圧縮に近づける
圧縮比の問題はゲージ圧力に注意。ゲージ圧力と大気圧を足した状態で計算する
「吸込み圧力が0.2MPa(ゲージ圧力)、吐き出し圧力0.8MPa(ゲージ圧力)である圧縮機の圧力比は4である」
(0.8+0.1)÷(0.2+0.1)=3
となるのでこの問題は不正解です。
ポンプについては
- ターボ形ポンプは遠心、斜流、軸流ポンプ
- ターボ形ポンプは吐き出し量が増えると揚程が低下し、効率は上昇して吐き出し量が100を超えた辺りで減少する。軸動力は遠心が低下し、斜流は変化せず、軸流は上昇する
- 容積形ポンプは往復、回転ポンプ
- 遠心ポンプの羽根車の出口に案内羽根のあるものはディフューザポンプ、ないものを渦巻ポンプ
- 往復ポンプの脈動を小さくする為にシリンダの数を増やすか吐き出し配管にアキュムレータを取り付ける
- ターボ形ポンプは低揚程大容量に適している
最後に

これで一通り終わりました。お疲れ様でした。
何度も申し上げますがこの記事とその他参考書を参考にして勉強に励んで下さい。
中々一回では覚えられないような内容ですが、時間を掛けてじっくり勉強しましょう。
では最後に一言
もう二度と勉強したくない

長い戦いお疲れ様でした!
各科目へのリンクはこちらからどうぞ
今回使用したのはこの2冊です。
この2冊ほぼ丸暗記で合格出来たので、これから受験される方は是非検討して見て下さい。









のバグ技-カプエス2-前キャン(RC)取得のコツ-120x68.png)
コメント
高圧ガス丙種化学•学識テストまで後3日の所で、コチラのブログに辿りつきました。
何でもっと早くに検索しとかなかったのか、悔やんでも悔やみきれません。
過去問と教本だけでは進みが遅く、理解がしにくく困っていました。
非常に分かりやすくて、文章が面白く、大変参考になりましたm(_ _)m
閲覧ありがとうございます。
高圧ガスの試験の情報が、あまりネット上にないので独学だと苦労しますよね…
学識は特に難易度が高く覚える事も多いので、受験者の負担を減らすべく最低限覚える所だけまとめました。少しでもお役に立てて幸いです。
試験まであと少しですが、落ち着いて頑張って下さい。合格を祈願しています(^^)
ネット上に液石の情報が多いのですが、特別化学に関する情報が少なく助かります。
既に液石は持っています。
今回、スカの過去問集を買ってしまったので余計にありがたいです。
オーソドックスな評価が高い方にしとけばよかった。。。。
1点、法令に関して「継承」と書かれていますが、法律や財務の世界では「承継」です。
高圧ガスの問題文も承継となっています。
できれば修正をお願いします。
ktak様
ご指摘ありがとうございます。確認しました所、確かに誤りでした。申し訳ございません。当該箇所は修正しましたのでよろしくお願いします。
少しでも勉強の助けになったのであれば幸いです。合格祈願しています。頑張って下さい。
協会のテキストで勉強していて技術検定を受けるつもりなのですが
技術検定の学識保安過去問メインで解いて国家試験の学識保安過去問は後回しで勉強しても大丈夫でしょうか
コメントありがとうございます。自分は全科目受験だったので、国家試験の過去問を完璧にするつもりで勉強しましたが、技術検定とは若干出題傾向が異なる可能性があります。
技術検定を受験するのであれば、まずは技術検定の過去問を中心に解いて余裕があれば国家試験の過去問で問題ないと思います。
今年、講習込みで受ける予定です。
とても分かりやすく大変助かってます。
ありがとうございます!
ところでこちらの
2023-2024年版 高圧ガス製造保安責任者試験 丙種化学(特別)攻略問題集
を繰り返しやりこんでますが、他のネットや本の問題集もやっておいた方がよろしいでしょうか。
コメントありがとうございます。自分が受験した時は丙特の参考書的なものが他に選択肢がなかったので、自分はこの1冊を丸暗記するくらいの気持ちでやり込みました。やはり過去問ノックが1番確実かと思います。試験頑張って下さいね。
すみません。
再度、質問です。
記事内の
この問題も先に断面積を求めて純粋に荷重から割れば求められます。
・0.026x0.026x3.14÷4=約0.00053㎡
・95÷0.00053=約180MPa
と、ありますが、
95/0.00053=179245 ですよね。
この公式の単位がPaとして 1Mpa = 1000000pa が、どうして 約180MPa になるのですか?
攻略問題集にも記載されていない基本的な事だと思うのですが、どうしても分かりません。
時間がある時にでも教えてくれると嬉しいです。
質問ありがとうございます。
まず、求めた計算は179245で間違いありません。引張荷重の単位がKNとあるので179245KPaとなります。KPaからMPaに直す場合1000で割る必要があるので179245÷1000=179.245MPaとなります。
また、記事内に記載していませんでしたが、この問題の選択肢が
(1)45MPa(2)65MPa(3)90MPa (4)135MPa (5)180MPa
この中で1番近い数値が180MPaなので約180MPaとなります。
分かりにくくて申し訳ありません。ご理解頂けましたでしょうか?
「引張荷重の単位がKNとあるので179245KPaとなります。」
こちらで理解出来ました。
ありがとうございました!